文部科学省科学研究費補助金「新学術領域研究」
新学術領域|ゲノム・遺伝子相関
月別アーカイブ
計画研究班別アーカイブ
公募研究班別アーカイブ
旧公募研究班別アーカイブ
「研究経過報告」内を検索
【東京大】小林班の記事を表示しています
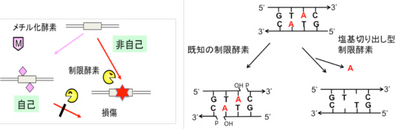
制限酵素は、特定のDNA配列の塩基がメチル化されていないときに、DNAを切断します。DNAを切るはさみとして、生命科学とバイオテクノロジーに大きな役割を果たしてきました。生命活動では、エピジェネティクスによる自己と非自己の区別によって遺伝的隔離による進化に寄与しています。
これまで知られている 制限酵素は全て、DNAのヌクレオチド単位を繋ぐリン酸ジエステル結合を加水分解します。私たちは、メチル化標的の塩基を切り出す新しい型の制限酵素を発見しました。
このような塩基切り出し酵素(DNAグリコシラーゼ)は、これまでDNA塩基損傷の修復で知られていましたが、最近動物細胞でDNAの脱メチル化に関わることが示されています。私たちの発見は、DNAメチル化によるエピジェネティクスの過程を繋げ、遺伝過程の理解を拡げるものです。
「ATGCという塩基配列で書かれたゲノム情報が、遺伝と進化の単位」というのが現在の生命観です。これに対して、「エピゲノム情報こそが、遺伝と進化の単位」ではないかと、私たちは考えました。エピゲノム情報の中でも、塩基配列に特異的な塩基メチル化が、遺伝子発現と適応的形質を変える可能性に注目しました。
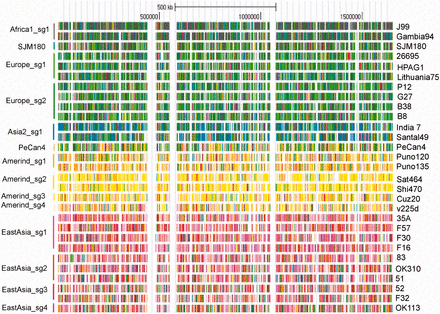
この「エピゲノム駆動進化仮説」をテストするために、ピロリ菌5株について、PacBio社の 一分子リアルタイムシーケンシング技術によって、ゲノム全域でメチル化塩基を一塩基の分解能で検出しました。(ピロリ菌と、その仲間は、ヒトと動物に胃がんなどの病気を起こす単細胞の細菌です。)
メチル化の配列特異性を担う遺伝子が、遺伝子内ドメイン配列移動(DoMo)という再編機構によって、メチル化配列を切り替えている事を証明しました。さらに、メチル化配列特異性遺伝子の有無が遺伝子発現に影響することを、トランスクリプトーム解析(IlluminaマシンによるRNA-seq)で、示しました。
本成果は「生物がエピゲノム状態を作り替えることで進化する」という「エピゲノム駆動進化」仮説を支持します。さらに、エピゲノムを標的とする「エピゲノム育種」への道を開きます。
Furuta,
Y. et al. PLoS Genetics, in press.
リボソームRNA遺伝子は、多くの遺伝子の中でもとりわけ保守的と見なされ、生物の系統分類に使われています。私たちは、リボソームRNA遺伝子の大規模な変異を、入手できる全ての細菌の完全ゲノム配列のバイオインフォマティクス解析によって、探しました。
「mRNAの5'部分にあるSD (Shine-Dalgarno) 配列と、16S RNAにある反SD配列が、ペアを作る」という翻訳開始の機構は、すべての細菌にあると信じられてきました。ところが、私たちは、「どの16S RNAにも、反SD配列のコア配列(5'-CCTCC-3')が無い」という細菌を発見しました。この喪失に対応して、遺伝子の上流のSD様配列の喪失が起きていました。
私たちは、また、大規模な再編を起こしたrRNA遺伝子を発見し、その形成過程を再構成しました。それらは、「逆位」、「重複」、「トランスポゾン挿入」、「欠失」、「置換」です。それらの背景には、「リボソームRNA転写と染色体複製の方向が同一になる選択」、「rRNA遺伝子の水平伝達」、「rRNA変異のゲノム内での遺伝子変換による広がり」という生物学的過程が推定できました。
これらの結果は、これまで見過ごされていた「リボソームRNA遺伝子とタンパク合成装置のダイナミックな進化の過程」を理解する出発点になるでしょう。
この論文は、Faculty of 1000に推薦されました。
Kyungtaek Lim, Yoshikazu Furuta, Ichizo Kobayashi. Large variations in bacterial ribosomal RNA genes. Molecular Biology and Evolution, epub ahead of print.
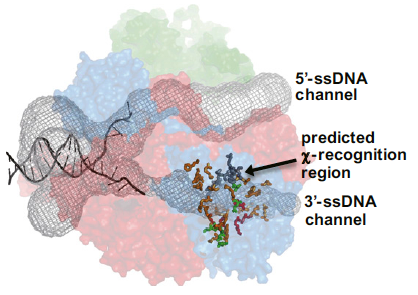
何が「自己」ゲノムで何が「非自己」ゲノムかを見分けるしくみは、ゲノムの維持に重要です。この生命活動の根本について、もっとも研究が進んでいる大腸菌では、「非自己」ゲノムを分解し、「自己」ゲノムを修復することが、RecBCDという酵素によって行われています。この酵素は、DNAに両鎖切断があると、そこからDNAの鎖をほどき分解しながら進んでいきますが、特定のID配列(カイ配列、5'-GCTGGTGG-3')があると、そこで分解をやめ、相同組換えによる修復に切り替えます。こうして、制限酵素などで切断された「非自己」のDNAは完全に分解され、複製フォークなどで切断された染色体(「自己」DNA)は修復されることになります。このID配列は、近くの相同組換えを促進する「組換えホットスポット」として発見されました。どういう配列がID配列になるかは、細菌の系統ごとに異なっています。
本研究では、この配列をこの酵素のどのような立体構造が認識して、反応様式の切り替えをもたらすかを、多数の変異体の解析によって明らかにしました。この結果は、「自己」「非自己」認識という生命の根元を、原子座標の分解能で理解する上での突破口になるでしょう。
Naofumi Handa, Liang Yang, Mark S. Dillingham, Ichizo Kobayashi, Dale B. Wigley, Stephen C. Kowalczykowski. Molecular determinants responsible for recognition of the single-stranded DNA regulatory sequence, χ, by RecBCD enzyme. Proc. Nat. Acad. Sci. USA, epub ahead of print.
http://www.pnas.org/content/early/2012/05/16/1206076109